國家藥品監(jiān)督管理局藥品審評中心(CDE)于2025年7月4日發(fā)布《關(guān)于公開征求藥品電子通用技術(shù)文檔(eCTD)相關(guān)技術(shù)文件和申報資料目錄層級對應(yīng)表意見的通知》,標(biāo)志著中國eCTD技術(shù)標(biāo)準(zhǔn)迎來首次技術(shù)層面的全面修訂。北京康茂峰科技有限公司eCTD電子提交業(yè)務(wù)負(fù)責(zé)人Richard迅速響應(yīng),通過“康茂峰醫(yī)學(xué)翻譯”視頻號對此次更新進(jìn)行專業(yè)解讀,助力行業(yè)及時把握政策動向。
《關(guān)于公開征求藥品電子通用技術(shù)文檔(eCTD)相關(guān)技術(shù)文件和申報資料目錄層級對應(yīng)表意見的通知》
與時俱進(jìn):與國際最新標(biāo)準(zhǔn)與現(xiàn)行實(shí)操接軌
Richard在視頻中指出,本次修訂以“與時俱進(jìn)”為主基調(diào),核心變化包括:
1、徹底告別紙質(zhì)要求:刪除所有與紙質(zhì)資料相關(guān)的條款,將“紙質(zhì)遞交”統(tǒng)一調(diào)整為“非eCTD方式遞交”,與當(dāng)前電子申報實(shí)際流程同步。 

實(shí)施指南 v1.1 (修訂版征求意見稿)中目錄刪除章節(jié)2.8 紙質(zhì)資料的遞交及要求


實(shí)施指南 v1.1 (修訂版征求意見稿)中章節(jié)4.1.2刪除說明函內(nèi)容中與紙質(zhì)資料內(nèi)容相關(guān)的部分


實(shí)施指南 v1.1 (修訂版征求意見稿)中將敘述中的“紙質(zhì)遞交”調(diào)整為“非eCTD方式提交”
2、國際規(guī)范升級:參考指導(dǎo)原則文件更新至最新版,包括《ICH eCTD文件格式規(guī)范》(1.2→1.3)和《ICH eCTD IWG問題解答和規(guī)范變更要求文件》(1.31→1.33),強(qiáng)化與國際標(biāo)準(zhǔn)接軌。


3、技術(shù)細(xì)節(jié)優(yōu)化:文件大小限制從500MB壓縮至200MB,與電子申報資料要求一致;新增“網(wǎng)絡(luò)傳輸”提交方式,提升操作靈活性;同步更新政務(wù)系統(tǒng)名稱及“電子簽章”等術(shù)語表述。


eCTD實(shí)施指南 v1.1 (修訂版征求意見稿)中將章節(jié)7.6中的單個文件大小從“500 MB”調(diào)整為“200 MB”


eCTD驗(yàn)證標(biāo)準(zhǔn) v1.1 (修訂版征求意見稿)中將2.2項(xiàng)中的單個文件大小從“500 MB”調(diào)整為“200 MB”


eCTD實(shí)施指南 v1.1 (修訂版征求意見稿)中2.7章節(jié)提交要求中增添“網(wǎng)絡(luò)傳輸”


eCTD實(shí)施指南 v1.1 (修訂版征求意見稿)中2.4章節(jié)將“國家藥品監(jiān)督管理局網(wǎng)上辦事大廳藥品業(yè)務(wù)應(yīng)用系統(tǒng)”調(diào)整為“國家藥品監(jiān)督管理局政務(wù)服務(wù)門戶藥品業(yè)務(wù)應(yīng)用系統(tǒng)”。


eCTD技術(shù)規(guī)范 v1.1 (修訂版征求意見稿)以及eCTD實(shí)施指南 v1.1 (修訂版征求意見稿)將“電子簽名”調(diào)整為“電子簽章”,與現(xiàn)行其他法規(guī)一致。
精益求精:技術(shù)要求優(yōu)化與范圍再擴(kuò)展
修訂的另一重點(diǎn)是對技術(shù)規(guī)范和適用范圍的精細(xì)化調(diào)整:
1、電子簽章要求簡化:僅保留1.0說明函、1.2申請表等6類關(guān)鍵文件需簽章,大幅減輕企業(yè)負(fù)擔(dān)。

2、驗(yàn)證標(biāo)準(zhǔn)升級:將部分與PDF大小、書簽以及超文本鏈接等驗(yàn)證項(xiàng)的嚴(yán)重程度從“警告”提升為“錯誤”,提高PDF文件的質(zhì)量要求。
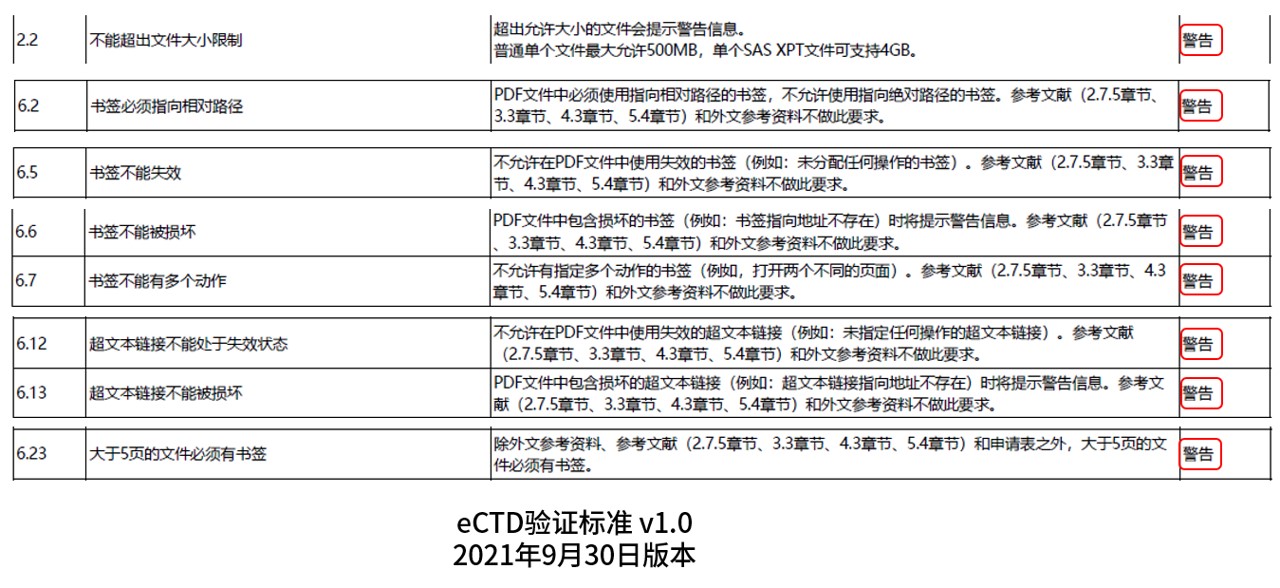
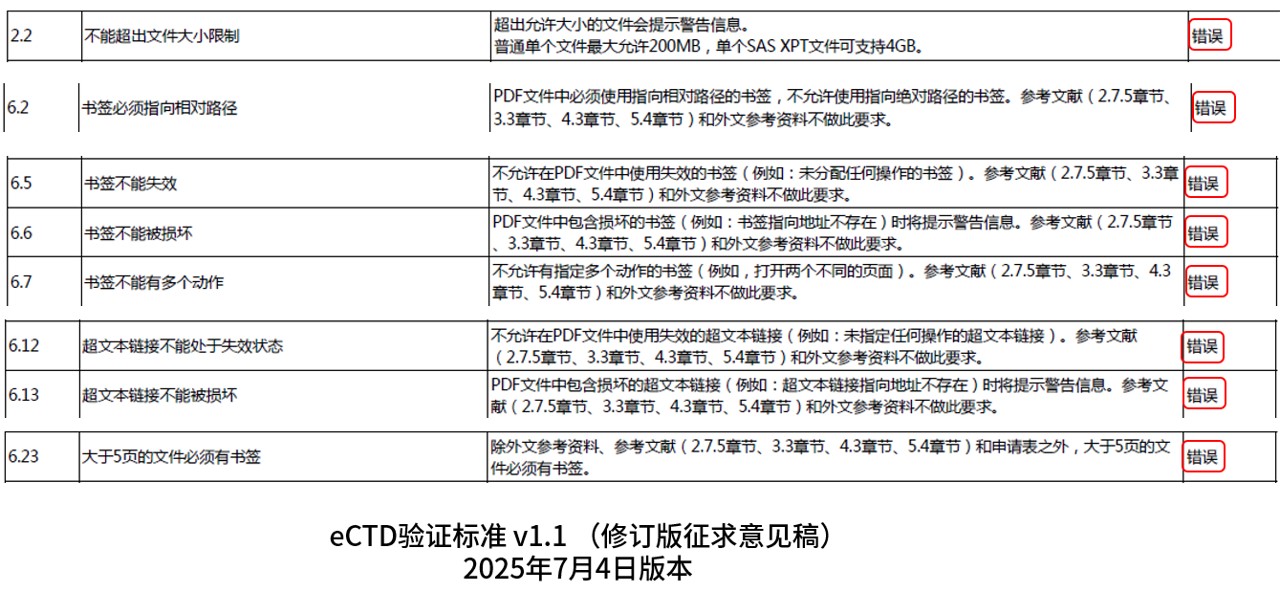
eCTD驗(yàn)證標(biāo)準(zhǔn) v1.1 (修訂版征求意見稿)中將8項(xiàng)與PDF相關(guān)的驗(yàn)證項(xiàng)的嚴(yán)重程度從“警告”提升到“錯誤”
3、適用范圍擴(kuò)容:新增原料藥、按生物制品管理的體外診斷試劑上市許可申請、一致性評價等申請的eCTD技術(shù)要求,為未來全類別覆蓋鋪路。




